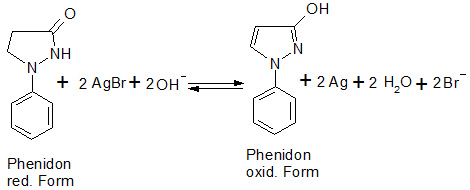
Chemische und physikalische Grundlagen der Schwarz-Weiß-Silberfotografie
(von Jens Vogel 2012)
1. Die EntwicklungDas bei der Belichtung entstandene noch nicht sichtbare "latente" Bild wird im Entwicklungsprozess sichtbar gemacht, eben "entwickelt". Im Entwicklungsprozess werden durch chemische Reduktion von Silber-Ionen weitere Silberatome gebildet, die sich an den bei der Belichtung entstandenen "Entwicklungskeim" anlagern. Diese "Cluster" wirken hierbei als "Kristallisationskeime", auf denen weitere Silberatome aufwachsen, bis schließlich ihre Größe so weit zunimmt, dass sie in der Summe als "schwarzer Punkt" sichtbar werden. Dieser Vorgang verläuft relativ langsam und ausschließlich dort, wo bei der Belichtung durch Auftreffen von Licht eben diese "Entwicklungskeime" vermehrt vorhanden sind.
Als Reduktionsmittel kommen eine Reihe chemischer Substanzen in Frage, in der Regel alles Derivate des Benzols, die in ortho- und para-Stellung entweder Hydroxyl-Gruppen oder Aminogruppen (oder beide) tragen. Alle Entwickler sind mehr oder weniger stark giftig (auch bei Hautkontakt durch Resorption) und meistens krebserregend (cancerogen). Es ist deshalb unbedingt notwendig mit Handschuhen zu arbeiten.
Die "klassischen" Entwickler sind die beiden Dihydroxibenzole Brenzkatechin (ortho-Dihydroxibenzol bzw. 1,2-Dihydroxibenzol) und Hydrochinon (para-Dihydroxibenzol bzw. 1,4-Dihydroxibenzol). Die Entwicklersubstanzen werden selber oxidiert zu chinoiden Bindungssystemen. Die 1,3-Derivate (Gruppen in meta-Stellung) lassen sich nicht oxidieren, sie können kein chinoides Bindungssystem aufbauen und sind als Entwickler ungeeignet.
Man verwendet wässrige Lösungen der Verbindungen, die je nach Verwendung des Entwicklers durch Zugabe von Soda (Natriumcarbonat) leicht, oder Kalilauge (Kaliumhydroxid-Lösung) stark alkalisch gemacht werden. Zusätzlich gibt man noch Natriumsulfit hinzu, welches die Oxidation der Entwicklersubstanzen durch Luftsauerstoff verhindert und auch die Lagerfähigkeit erhöht. Natriumsulfit ist selbst auch ein Reduktionsmittel, ist aber nicht in der Lage, Silberbromid zu reduzieren, wohl aber den Luftsauerstoff.
Die Zugabe von Kaliumbromid verhindert die Schleierbildung, Komplexbildner, (z.B. EDTA - Etyldiamintetraacetat)) binden evtl. im Wasser vorhandene Schwermetallionen und bei hartem Wasser Calcium- bzw.Magnesiumionen.
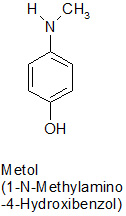
Sehr weit verbreitet sind Entwickler auf der Basis von Metol (s.u.)2. Die chemischen Hintergründe der Entwicklung
Die chemischen Hintergründe der Entwicklung sollen hier am Beispiel des Hydrochinons erklärt werden. Andere Entwicklersubstanzen (s.u.) arbeiten im Prinzip ähnlich.
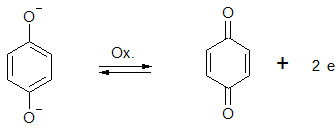
Oxidation und Reduktion sind chemische Reaktionen, die immer gleichzeitig nebeneinander ablaufen und die mit der Abgabe bzw. Aufnahme von Elektronen verbunden sind, sog. Redoxreaktionen. Silberionen aus dem Silberbromid-Gitter werden zu elementarem Silber reduziert, sie nehmen hierbei jeweils ein Elektron auf. Das notwendige Elektron stammt aus dem Reduktionsmittel (hier als Beispiel Hydrochinon), welches oxidiert wird und hierbei Elektronen abgibt.
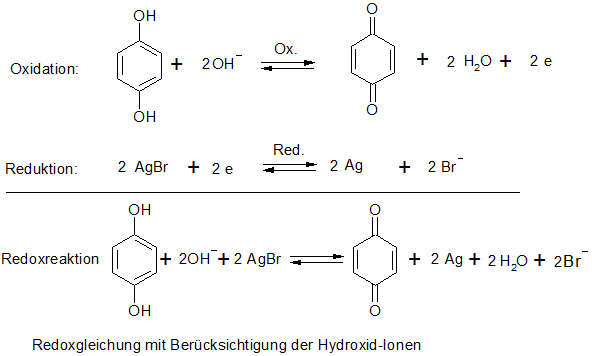
Der Entwicklungsvorgang lässt sich durch folgende chemische Reaktionsgleichungen wiedergeben:
Oxidation und Reduktiuon werden formal als Teilvorgänge (Teilgleichungen) dargestellt, zusammengefasst ergeben sie die Gesamtgleichung (Redoxgleichung).
a. Reduktion von Silberbromid (Elektronenaufnahme)
(reduziert werden eigentlich nur die Silber-Ionen. Durch Aufnahme eines Elektrons wird das positiv geladene Ag+ - Ion zum ungeladenen Silberatom. Da das Reduktionsmittel (s.u.) zwei Elektronen zur Verfügung stellt, können zwei Ag+ - Ionen reduziert werden).Die Bromid-Ionen bleiben unverändert)
b. Oxidation von Hydrochinon (para-Dihydroxibenzol, 1,4-Dihydroxibenzol)
Hydrochinon wird hierbei zum Chinon (para-Benzochinon) oxidiert und gibt zwei Elektronen ab. Im alkalischen Medium liegt das Hydrochinon in Form seines Dianions vor, es wurden also vorher zwei Protonen ( H+-Ionen) abgegeben.
c. Zusammenfassung der Teilvorgänge zur Gesamtgleichung
(Redoxreaktion)
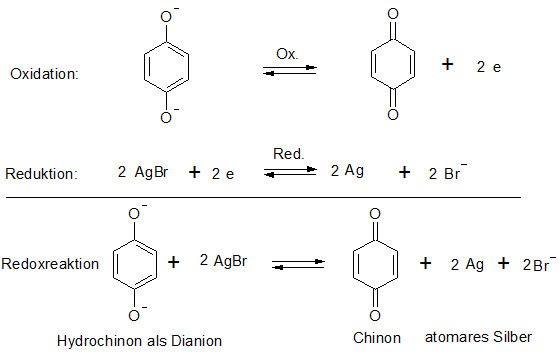
Ausgehend von Hydrochinon und unter Berücksichtigung der anwesenden Kalilauge (alkalisches Medium) ergibt sich alternativ folgende Redoxgleichung:
Das bei dieser Reaktion gebildete atomare Silber wächst auf den Entwicklungskeimen auf und bildet dort einen mehr oder weniger großen sichtbaren schwarzen "Punkt", in der Summe entsteht das sichtbare Bild.
Die Entwicklungszeit ist abhängig von der Konzentration der Entwickler-lösung, vom pH-Wert und vom zu entwickelnden Material. Stärker alkalische Entwicklerlösungen arbeiten "härter" und schneller , verdünnte Lösungen arbeiten weicher und langsamer.
3. Unterbrecherbad (Stoppbad)
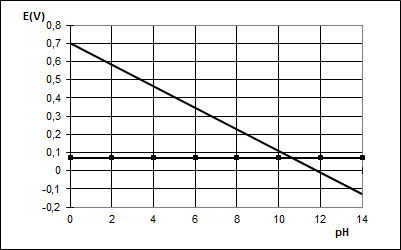
Nach beendeter Entwicklung gibt man das Bild vorübergehend in das sog. "Stoppbad", meistens eine ca. 2%ige Essigsäure-Lösung. Hier wird der pH-Wert auf ca. 3 herabgesetzt, der Entwickler verliert seine reduzierende Eigenschaft, der Entwicklungsprozess wird unterbrochen.
(vergl. neben stehendes Diagramm). Danach folgt die Fixierung.